البوليمرات الحيوية الميكروبية الواعدة مصادرها، الخلفية الوراثية والتطبيقات التقنية
البوليمرات الحيوية
البوليمرات الحيوية، التي أصبحت ذات قيمة للاستخدام في الكثير من التطبيقات، تتفوق على المشتقات البتروكيماوية في كونها قابلة للتحلل الحيوي ومتوافقة حيويًا وبيئيًا.
السكريات هي نوع آخر من الجزيئات الكبيرة الموجودة على نطاق واسع في الطبيعة. يمكن فصلها بناءً على مورفولوجيا توطينها كجزء من الغشاء السيتوبلازمي أو على شكل عديدات السكاريد داخل الخلايا داخل جدار الخلية أو على شكل عديدات السكاريد خارج الخلية خارج جدار الخلية.
تحتوي السكريات خارج الخلية على بنيتين: فهي لا تلتصق بالخلايا، وتشكل مخاطًا فضفاضًا وتجعلها لزجة؛ عندما تتطور البكتيريا في الوسائط الصلبة أو السائلة، فإنها تأخذ شكلًا لزجًا وتشكل ملتصقة بكبسولات جدار الخلية أو كبسولات دقيقة. لديهم هياكل وحدود فريدة ولا تنفصل إلا تدريجيًا في المحاليل الملحية أو المائية. لذلك، يمكن فصل الكبسولات الدقيقة والكبسولات عن المخاط السائب عن طريق الطرد المركزي (Wilkinson, 1958).
عديدات السكاريد الخارجية هي عديدات سكاريد طويلة السلسلة تتكون من وحدات سكر متفرعة متكررة أو مشتقات السكر، بشكل رئيسي الجالاكتوز والرامنوز والجلوكوز بنسب متفاوتة. وهي مقسمة إلى مجموعتين: عديدات السكاريد غير المتجانسة (صمغ الزانثان وصمغ الجيلان) والسكريات المتجانسة (الكردلان، والديفورمان، والسليلوز، والجلوكان والأميلوبكتين). (Sutherland, 1994)
تتكون عديدات السكاريد المتجانسة من نوع واحد فقط من السكريات الأحادية (D-فركتوز أو D-جلوكوز) المرتبطة بعدد ثابت من مجموعات أنواع الروابط أو أنواع الروابط الفردية. تتكون عديدات السكاريد المتغايرة من عدة نسخ من سكريات قليلة التعدد تحتوي على 3 إلى 8 بقايا ينتجها كائن حي دقيق آخر. للسكريات الخارجية العديد من التطبيقات الصناعية في الصناعات الدوائية والغذائية وغيرها من الصناعات مثل مستحضرات التجميل وعوامل التبلور وأدوية تضميد الجروح والورق والمنسوجات((Sutherland, 1998
الأمثلة المهمة في السكريات الأحادية هي السليلوز. السليلوز هو البوليمرات الحيوية الأكثر أهمية، ويتم إنتاجه بشكل أساسي عن طريق النباتات. ومع ذلك، يمكن لبعض أنواع البكتيريا أيضًا إنتاج السليلوز بتركيبة كيميائية تشبه تركيبة السليلوز النباتي ولكن بخصائص فيزيائية فريدة. يرجع هذا الاختلاف إلى أن الشبكة الشبكية لأليافها الدقيقة التي يبلغ قطرها (0.1 م) تساوي حوالي 100 من ألياف الخشب.
أيضًا، على عكس السليلوز النباتي، لا يحتاج السليلوز الميكروبي إلى تحويل إضافي ,تم إخلاؤها من ملوثات وشوائب غير مرغوب فيها مثل البكتين والهيميسيلولوز واللجنين، وبهذه الطريقة يكون لديه خيار الاحتفاظ بمستوى بلمرة بارز(Nishi et al. 1990) .
السليلوز الميكروبي
أثبت السليلوز الميكروبي أيضًا خصائص منفردة، كما هو الحال من حيث النقاء، وقوة الشد، ومعامل يونج أعلى من الألياف الاصطناعية بحوالي 30-40? (Tanskul et al. 2013)، والقدرة على التورم بما يصل إلى 700 مرة من أليافها. الوزن الجاف. يتميز هيكل أليافه بنعومة تتراوح من 0.1 إلى 10 ميكرومتر وبلورة عالية وتحلل أفضل من السليلوز من النباتات (Cai and Kim, 2010). وفي الوقت نفسه، يحتوي السليلوز المستخرج من النباتات على اللجنين والبكتين والهيميسليلوز كمركبات رئيسية. مما يجعلها أكثر ملاءمة كمادة خام لإنتاج الورق عالي الجودة والأطعمة الحلوى ومكبرات الصوت عالية الدقة (Shoda and Sugano, 2005). ألياف السليلوز البكتيرية أرق بنحو 100 مرة من ألياف السليلوز النباتية، وبالتالي فهي مادة مسامية للغاية، مما يسمح بنقل الأدوية أو المضادات الحيوية المختلفة إلى الإصابة بينما تعمل في نفس الوقت كحاجز مادي عاطفي مقابل أي تلوث خارجي. لذلك، يتم استخدامه على نطاق واسع في شفاء الإصابات (Czaja et al. 2006).
لقد أصبح السليلوز البكتيري مؤخرًا سمة مميزة للعديد من المنتجات الطبية الحيوية المهمة بما في ذلك زراعة الأوعية الدموية (الأنابيب)؛ ضمادات العناية بالجروح؛ الخيوط الجراحية يزرع متوافقة حيويا. ومصفوفات تقوية الأنسجة إلى جانب الصناعات التقليدية الأخرى مثل الورق؛ منتجات الطعام؛ الإلكترونيات ومنتجات التجميل.إذ وجد أنه يتميز عن السليلوز النباتي من حيث التجدد والتحلل الحيوي إلى جانب خواصه الميكانيكية الفريدة بما في ذلك درجة التبلور العالية؛ نقاء؛ سعة تخزين الماء؛ التوافق الحيوي والمرونة لقد كانت كولومبيا البريطانية هدفاً جذاباً للإنتاج التجاري في السنوات الأخيرة. (Naomi et al., 2020; Zhong C (2020)
السلالات البكتيرية المنتجة للسليلوز
كما أن الكائنات الحية الدقيقة التي تنتج السليلوز لها تطبيقات وخصائص مختلفة عن السليلوز النباتي. يتم إنتاج السليلوز بواسطة الكائنات الحية الدقيقة المختلفة مثل الطحالب والبكتيريا والفطريات. في الطحالب الخضراء، يعمل المنان والزيلان والسليلوز كهيكل لجدار الخلية من السكريات. على الرغم من أن السليلوز يتم إنتاجه بكميات صغيرة في معظم الطحالب الحمراء (Rhodophyta)، وفي جميع الطحالب البنية (Phaeophyta) وفي نهاية المطاف من الطحالب الذهبية (Chrysophyta) (Richmond, 1991). في Oomycetes، يتم استبدال الكيتين بالكامل بالسليلوز الذي يمثل حوالي 15? من الكتلة الجافة للجدار. كما أن الأنواع سالبة الجرام مثل Alcaligenes، Azotobacter، Acetobacter، Sarcina، Rhizobium، Pseudomonas، Salmonella، Agrobacterium، Achromobacter، Aerobacter كانت تنتج السليلوز
Morgan et al. 2013).). علاوة على ذلك، يتم تصنيع السليلوز بواسطة بكتيريا Sarcina ventriculi وهي بكتيريا إيجابية الجرام، تمثل حوالي 15% من إجمالي كتلة الخلايا الجافة.
تخليق السليلوز البكتيري:
يعد تخليق السليلوز البكتيري عملية دقيقة ومنظمة بشكل خاص وتتضمن العديد من الخطوات. كما هو مبين في الشكل 5؛ إن البنية فوق الجزيئية لمجمع يحتوي على عدد كبير من البروتينات التحفيزية والتنظيمية بالإضافة إلى الإنزيمات الفردية ليست واضحة بعد. إن آلياتومسارات تخليق الجلوكوز ثنائي فوسفات اليوريدين (UDPGlc) معروفة جيدًا نسبيًا، في حين أن الآلية التي يتبلمر بها الجلوكوز إلى سلاسل طويلة غير متفرعة لا تزال بحاجة إلى التحقيق (.،Prashant et al 2009).
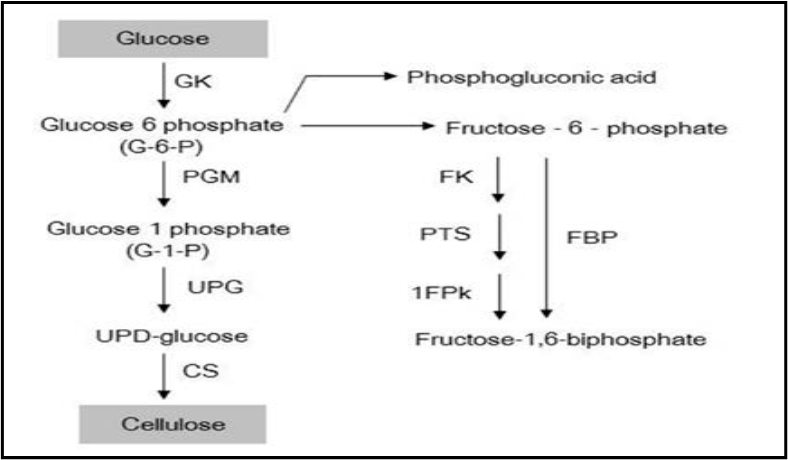
الشكل : - مسار تصنيع السليلوز البكتيري لبكتيريا Acetobacter sp. 1FPk (فركتوز-1-فوسفاتكيناز)، PTS (نظام نقل الفوسفات)، FBP (فركتوز-1،6-ثنائي فوسفات فوسفات)، FK (فركتوكيناز)
هيكل السليلوز البكتيري
الصيغة الجزيئية (C6H10O5)n للسليلوز البكتيري هي نفس صيغة السليلوز النباتي، لكن خواصه الفيزيائية والكيميائية مختلفة. البنية الأساسية للسليلوز البكتيري عبارة عن بوليمر من سلاسل الهيدروجين المرتبطة بإحكام بين مجموعات الهيدروكسيل، تسمى الميكروفيبريلز، بسمك 3-8 نانومتر وعرض 50-80 نانومتر، مع سلاسل جلوكان متصلة من الداخل إلى الخارج. تم عرض هذه البنية الليفية الدقيقة للسليلوز البكتيري لأول مرة في عام 1949 بواسطة موليثالر، الذي أثبت أن كل سلالة بكتيرية تنتج بنية سليلوزية مختلفة.
الجينات المسؤلة عن انتاج السليلوز الميكروبي
في السلالات البكتيرية المنتجة للسليلوز. وأبرزها Gluconoacetobacter hansenii، ويتم تنظيم عملية التخليق الحيوي قبل الميلاد بواسطة أربعة جينات؛ وهي A وB وC و D التي تشتمل على أوبرا سينسيز السليلوز البكتيري (bcs) بطول 9.2 كيلو بايت، يسبقه شظايا "تنظيمية" يُقال إنها ضرورية للتخليق الحيوي قبل الميلاد؛ جين cmcax الذي يشفر إنزيم endo-β- 1,4-glucanase الذي يتحلل BC ويحسن تركيبه، وجين ccpAx الذي يعتقد أنه يلعب دورًا مهمًا في النقل خارج الخلية لـ (Thakur et al., 2020). يتم تشفير إنزيم سينسيز (تكوين الناتج المحلي الإجمالي) الرئيسي (PF03552) بواسطة جزء bcsA، بينما يقوم bcsB بتشفير بروتين تنظيمي ينتمي إلى فصيلة BcsB الفائقة (pfam03170) الذي يشفر البروتين التنظيمي للتخليق الحيوي للسليلوز والذي يُعتقد أنه يربط المستجيب الإيجابي لـ di-GMP الدوري. (Yin et al., 2009); ؛ كلاهما يشتمل على وحدة ترانسفيراز الجليكوزيل المعقدة المسؤولة عن نقل بقايا الجلوكوزيل من الجلوكوز UDP إلى سلسلة 1،4 جلوكان (Knott et al., 2016). وفي الوقت نفسه ، يُعتقد أن الأجزاء bcsC (InterPro: IPR001440) و D (InterPro: IPR022798) متورطة في تصدير وتعبئة ألياف السليلوز خارج الخلية من خلال تشكيل قناة إلى الغشاء الخارجي مما يسمح ببلورة . (Mehta et al., 2015). أفادت العديد من الدراسات أن شظايا bcsAB فقط هي الكافية لإنتاج فعال قبل الميلاد في المختبر (Omadjela et al., 2013) ومع ذلك، أكدت دراسات أخرى ضرورة الجينات الأربعة لتحقيق أقصى إنتاج داخل الجسم الحي (Vijayendran et al., 2020)
بحثت العديد من الدراسات في الإنتاج واسع النطاق لـ BC في العديد من الأنظمة القائمة على البلازميد (Omadjela et al., 2013; Costa et al., 2017; Buldum et al., 2018). في هذا المجال، يتم استخدام منصة E. coli على نطاق واسع كمنتج بروتين عالي الجودة بسبب حركية نموها السريع؛ التلاعب الجيني البسيط والتعبير السريع للبروتين، وما إلى ذلك (Sezonov et al., 2007). تشمل العوائل البكتيرية الأكثر استخدامًا لإنتاج البروتينات المؤتلفة على نطاق واسع سلالات E. coli B [Rosetta وBL21 (DE3)] وسلالات K-12، بما في ذلك سلالة تكرار البلازميد الرئيسية DH5α (Marisch et al., 2013). ومع ذلك، باعتباره بروتينًا مرتبطًا بالغشاء؛ تم الإبلاغ عن أن الإفراط في التعبير عن سينسيز السليلوز في E. coli BL21 (DE3) سام، مما يمهد الطريق لمضيفين بديلين آخرين مثل C41 (DE3). تم استخدام سلالة متحولة مشتقة من BL21 (DE3) لدراسة إمكانية التعبير الهائل عن بروتينات الغشاء السام من أوبرا bcs.، (Buldum et al., 2018
الخلاصة
السليلوز البكتيري عبارة عن مادة حيوية صديقة للبيئة وقابلة للتحلل الحيوي ولها خصائص فريدة أهلتها لتلقي اهتمام متزايد للعديد من التطبيقات الصناعية. ومع ذلك، فإن الإنتاج الضخم للسليلوز البكتيري باستخدام النوع البري المنتج للسليلوز لا يزال يواجه تحديًا بسبب حركية النمو البطيئة، والكمية الكبيرة من الجلوكوز المطلوبة للإنتاج الفعال، والقابلية الشديدة للطفرات التلقائية المرتبطة بتقلبات ظروف المنبت الغذائى /النمو التي تجعلها غير منتجة. الطفرات، وانخفاض إنتاجية السليلوز.
